Новости
7 июня 2022 г. состоится консультация высококвалифицированного врача-кардиолога по поводу заболеваний сердечно-сосудистой системы у переболевших COVID-19
30.05.2022 г. состоится консультация высококвалифицированного врача — невролога по поводу заболеваний нервной системы у переболевших COVID-19
20 мая 2022 г. состоится акция по бесплатному консультированию врачами-сурдологами
С наступающим Днем Победы!
УТВЕРЖДЕН НОВЫЙ ПОРЯДОК НАЗНАЧЕНИЯ ИНВАЛИДНОСТИ

Правительство РФ утвердило новые правила назначения и подтверждения инвалидности, которые вступят в силу 1 июля 2022 года.
До этого времени в России действует упрощенный порядок проведения медико-социальной экспертизы (МСЭ), позволяющий проходить процедуру только заочно.
После введения нового регламента граждане смогут сами выбирать очный или дистанционный формат МСЭ, с 1 июня 2023 года – заочно обжаловать результаты экспертизы в профильных бюро.
Кроме того, с 2024 года персональные данные россиян, получающих справки об инвалидности, будут предоставляться в бюро МСЭ и клиники в обезличенном виде.
С 1 июля 2022 года граждане получат возможность выбирать между двумя форматами прохождения МСЭ, но новый порядок также устанавливает перечень случаев, когда присутствие человека на МСЭ будет обязательным.
В него входит: несоответствие между данными медицинских исследований и заключением врачей, направивших гражданина на МСЭ, проживание пациента в интернате, корректировка программы реабилитации, необходимость обследования с применением диагностического оборудования.
Постановление правительства с 1 июня 2023 года вводит возможность дистанционного обжалования решений бюро МСЭ.
Такой формат будет доступен в учреждении по месту жительства, где гражданину предоставят возможность связаться со специалистами главного или федерального бюро МСЭ.
Новый порядок также предполагает, что с 1 января 2024 года заочная экспертиза будет проводиться без доступа сотрудников МСЭ и медорганизаций к персональным данным.
С помощью информационной системы обезличенные документы будут распределяться в бюро разных регионов, вне зависимости от места жительства гражданина.
Итоговое решение будет доступно на портале госуслуг либо направляться на бумажном носителе по почте.
Персональные данные будут отражаться только в готовой справке об инвалидности с указанием назначенной группы.
Обжаловать решение экспертизы гражданин сможет в бюро МСЭ по месту жительства.
Новые правила заменят действующий с апреля 2020 года порядок, введенный из-за связанных с COVID-19 ограничений.
Этот регламент позволил гражданам автоматически продлевать установленную инвалидность на шесть месяцев, разрешил назначать инвалидность и программу реабилитации дистанционно, после заочного прохождения МСЭ.
До утверждения временного порядка был разрешен только очный формат МСЭ.
В феврале 2022 года правительство продлило временный порядок проведения МСЭ до 1 июля.
МИЛАНА БОРОДИНА
Источник: Правительство РФ
https://vademec.ru/news/2022/04/06/utverzhden-novyy-poryadok-naznacheniya-invalidnosti-/
FDA РАСШИРИЛО ПОКАЗАНИЯ К ПРИМЕНЕНИЮ CAR-T-ТЕРАПИИ ОТ GILEAD
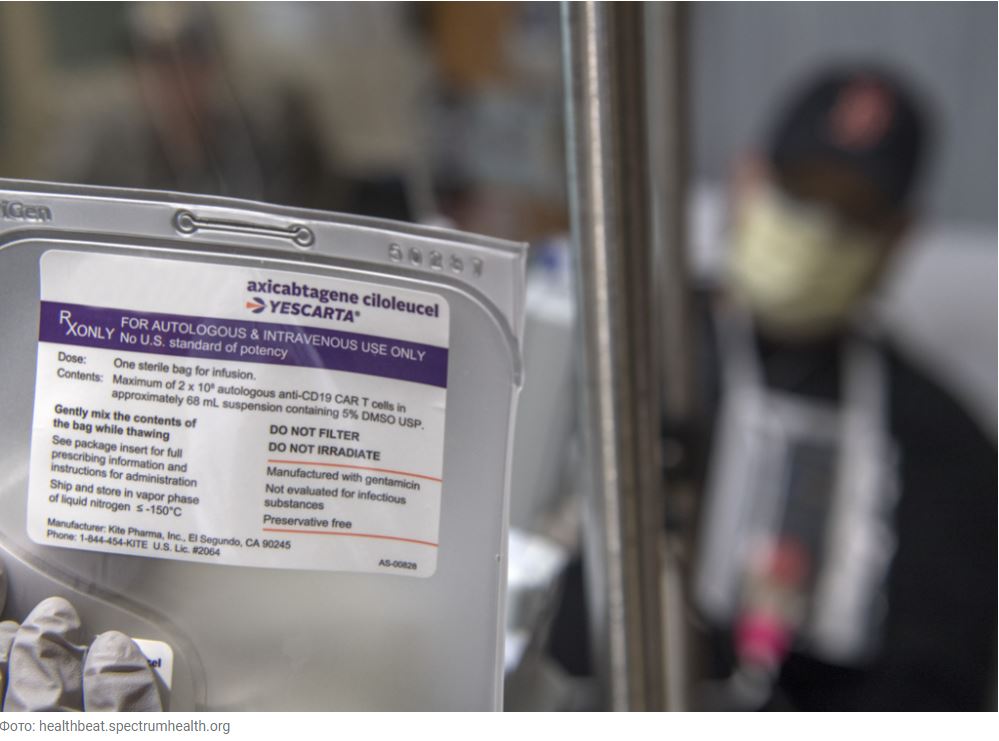
Управление по контролю за продуктами и лекарствами США (FDA) 1 апреля расширило показания к использованию препарата на основе технологии CAR-T – Yescarta (axicabtagene ciloleucel) – от Gilead Sciences.
Регулятор разрешил применять Yescarta для терапии диффузной В-крупноклеточной лимфомы в запущенной форме у взрослых, проявивших резистентность к химиоиммунотерапии первой линии, а также в случае рецидива у пациентов в течение года после прохождения такой терапии.
Расширение показаний к применению препарата Yescarta увеличит число пациентов, которые смогут пройти терапию, с 8 до 14 тысяч человек, отметила исполнительный директор одного из подразделений Gilead Кристи Шоу.
Изначально FDA одобрило CAR-T-терапию от Gilead в 2017 году.
Регулятор выдал разрешение на применение препарата при терапии диффузной В-крупноклеточной лимфомы у пациентов, не ответивших на две или более линий терапии.
Разработчиками еще двух коммерческих продуктов CAR-T являются Novartis (Kymriah) и Johnson & Johnson (Carvykti).
Препарат от Johnson & Johnson зарегистрирован для терапии множественной миеломы в США и Европе. CAR-T терапия от Novartis одобрена в США, Европе, Японии, Австралии, Сингапуре, Канаде и Южной Корее по показаниям «острый лимфобластный лейкоз» и «B-клеточная лимфома».
В России ни один из коммерческих продуктов CAR-T-терапии не зарегистрирован.
В стране ведутся собственные академические разработки такой терапии, но в марте 2022 года с ними возникли трудности.
СОФИЯ ПРОХОРЧУК
Источник:Gilead
https://vademec.ru/news/2022/04/04/fda-rasshirilo-pokazaniya-k-primeneniyu-car-t-terapii-ot-gilead-/








