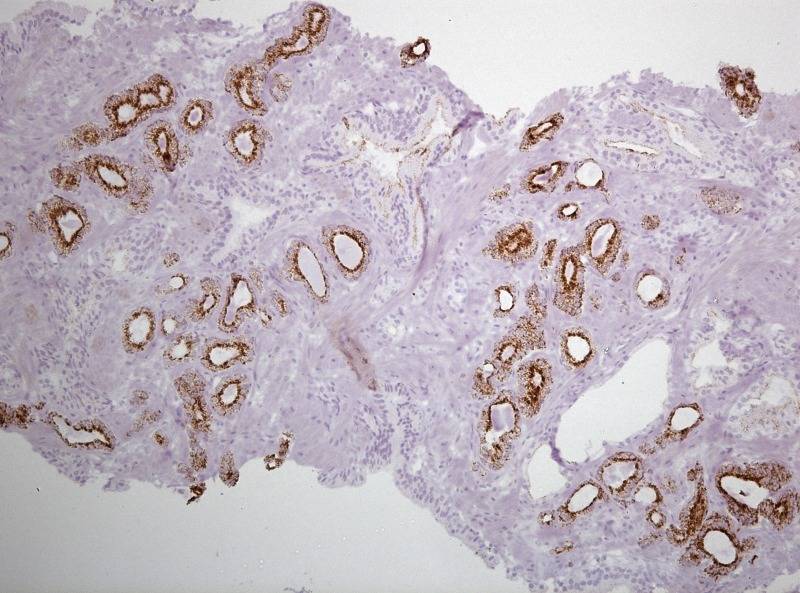
Иммуногистохимические методы используются для выявления локализации того или иного клеточного или тканевого компонента (антигена) in situ посредством связывания его с мечеными антителами и являются неотъемлемой частью современной диагностики рака, обеспечивая обнаружение локализации в тканях различных клеток, гормонов и их рецепторов, ферментов, иммуноглобулинов, компонентов клеток и отдельных генов.
Метод ИГХ нашел свое применение и в диагностике рака простаты. Маркеры рака предстательной железы выполняют 2 функции: используются для диагностики РПЖ и определяют потенциал злокачественности РПЖ. Определенные виды маркеров выполняют как одну, так и другую функцию (PSA, PSAP).
К маркерам, выполняющим диагностическую функцию, относят:
— цитокератины (общий цитокератин, СК-5/6, высокомолекулярный цитокератин) и маркер р63. Они экспрессируются базальным слоем эпителия. При РПЖ их экспрессия подавлена, они определяются в базальном эпителии доброкачественных структур предстательной железы.
— альфа-метилацил-КоА-рацемаза (AMACR). Повышение концентрации AMACR усиливает свободно радикальные процессы в клетке и повреждение ДНК. Скорее всего это объясняет повышенный риск РПЖ при высоком уровне поступления разветвленных жирных кислот с пищей (например, с молочными продуктами или говядиной). Высокоэффективен при иммуногистохимическом исследовании и позволяет дифференцировать рак от других патологических процессов, а также более точно определить стадию заболевания, в том числе и в биопсийном материале. Этот маркер считается позитивным в 80-100% случаев малых очагов рака. Используется совместно с р63 маркером базальных клеток, что обеспечивает эффективность 92-97%.
— хромогранин А, синаптофизин, серотонин. Используются для нейроэндокринной дифференцировки.
— простатспецифический антиген (PSA). Синтезируется секреторным эпителием ПЖ при участии дигидростерона. PSA экспрессируется во всех аденокарциномах предстательной железы. Снижение или отсутствие экспрессии PSA констатируется при низкодифференцированном раке. При некоторых аденокарциномах экспрессия PSA исчезает после проведения гормонотерапии или лучевой терапии.
— простатическая кислая фосфотаза (PSAP). Ее экспрессия весьма близка к экспрессии PSA. Оба маркера особенно пригодны для дифференциальной диагностики рака простатического происхождения с опухолями другого генеза, а также для определения исходной локализации опухоли при метастазах. В редких случаях, когда в аденокарциноме предстательной железы экспрессируется только один из этих двух маркеров, именно экспрессия PSAP чаще всего сохранена.
— простатспецифический мембранный антиген (PSMA). Используется, когда отсутствует экспрессия PSA и PSAP.
— андрогены и эстрогены. Обладают способностью стимулировать пролиферативные процессы в предстательной железе. Для андрогенов основной тканью-мишенью является эпителий, а для эстрогенов соединительная и мышечная строма предстательной железы. Используются для предсказания чувствительности к гормонотерапии.
Для определения потенциала злокачественности используют:
— Ki-67. Ген, кодирующий Ki-67, расположен на длинном плече 10 хромосомы. Ki-67 относится к регуляторным белкам. Стадия РПЖ напрямую соотносится с количеством опухолевых клеток, экспрессирующих Ki-67, поэтому индекс Ki-67 является независимым показателем прогноза рецидива и выживаемости у больных РПЖ.
— bcl-2 и р53. Ген р53 локализуется в ядре клетки, является супрессором опухолевого роста, предотвращая вступление клетки с поврежденной ДНК в синтетическую фазу цикла и индуцируя апоптоз. Мутация гена р53 ведет к потере контроля пролиферации клеток, угнетению апоптоза. Утрата функции этого гена может быть связана с высоким метастатическим потенциалом опухоли и развитием андрогеннезависимого РПЖ. Наличие мутаций в гене р53 в сочетании с повышенной экспрессией белка Bcl-2 при РПЖ является неблагоприятным прогностическим фактором течения заболевания. Также нарушение экспрессии р53 коррелирует со снижением выживаемости после простатэктомии. Белки семейства Bcl (Bcl-2 и Вах) играют ключевую роль в регуляции процессов апоптоза. Они индуцируют или ингибируют апоптоз в клетках ПЖ. Ген Вс1-2 может задерживать апоптоз клеток ПЖ, вызванный р53 и другими стимуляторами, в том числе цитостатическими препаратами. В случае гиперэкспрессии ген Bcl-2 выступает в качестве онкогена. В ткани ПЖ в норме экспрессия Bcl-2 осуществляется только клетками базального слоя эпителия. В андрогеннезависимом РПЖ отмечается усиленная экспрессия гена Bcl-2, что является признаком гормоноустойчивости и резистентности к индукторам апоптоза.
— кадгерин Е и бетакатенин. Кадгерины являются мембранными гликопротеидами и играют важную роль в кальцийзависимой межклеточной адгезии. Считается, что утрата межклеточных «мостиков» и связи с соседними эпителиальными клетками является одним из первых этапов развития опухоли. Снижение экспрессии Е-кадгерина нередко наблюдается при РПЖ и коррелирует с выживаемостью, клинической и морфологической стадией заболевания.
— белки p21 и p27. Являются опухолевыми супрессорами и ингибируют все типы циклин-зависимой киназы (cyclin dependent kinase CDK), препятствуя вступлению клетки в очередную фазу цикла деления. Мутации генов, кодирующих р21 и р27, встречаются при раке предстательной железы достаточно часто и коррелируют с неблагоприятным прогнозом заболевания. Иммуногистохимическая экспрессия p21/p27 коррелирует с длительностью безрецидивного течения, выживаемостью, степенью местной инвазии, поражением регионарных лимфоузлов.
— pRb. Играет важную роль в регуляции клеточного цикла. Утеря гетерозиготности локуса Rb наблюдается более чем в 60% случаев РПЖ.
Отдельной подгруппой идут факторы роста, которые при проникновении в ядро клетки обладают способностью стимулировать или ингибировать деление и дифференцировку клеток:
— рецептор эпидермального фактора роста (EGFR). Трансмембранный гликопротеин, обладающий тирозинкиназной активностью. EGFR экспрессируется на поверхности как нормальных, так и трансформированных эпителиальных клеток и участвует в регуляции клеточного роста и дифференцировки. Экспрессия EGFR при РПЖ достигает 40%.
— инсулиноподобный фактор роста (IGF). Является одним из основных факторов роста в ПЖ, ответственных за фазу синтеза ДНК. Выработка IGF эпителиальными клетками ПЖ по аутокринному типу является одним из изменений, происходящих одновременно с развитием РПЖ. IGF способен усиливать локальное действие андрогенов. Определение IGF иммуногистохимическим методом в ткани с помощью моноклональных антител. Выявлена достоверная положительная корреляционная связь между степенью злокачественности опухоли и экспрессией IGF при РПЖ.
— фактор роста эндотелия сосудов (VEGF). Мультифункциональный цитокин, вызывающий пролиферацию и миграцию эндотелиальных клеток, в том числе и при РПЖ. Повышает способность эндотелиальных клеток к миграции, а опухолевых клеток к инвазии и метастазированию. При доброкачественной гиперплазии предстательной железы (ДГПЖ) экспрессия VEGF в опухоли ниже, чем при РПЖ, и наблюдается в менее чем 5% клеток.
— интерлейкин-8 (ИЛ-8). Является фактором роста с паракринным и аутокринным механизмом действия. Синтез ИЛ-8 осуществляется нейроэндокринными клетками ПЖ. Интерлейкин-8 и его рецептор CXCR1 при ДГПЖ, простатической интраэпителиальной неоплазии и андрогензависимом РПЖ иммуногистохимически не экспрессируется. В случае развития андрогеннезависимого РПЖ отмечается экспрессия рецепторов к ИЛ-8 CXCR2, что указывает на роль местных тканевых факторов роста в процессах пролиферации клеток РПЖ.
https://unim.su/blog/igh-v-diagnostike-raka-predstatel-noj-zhelezy/